Le macchine filler stick, progettate per il riempimento di bustine monodose in formato stick, rappresentano una soluzione all’avanguardia per il processo di confezionamento di polveri, liquidi e granuli in modo sicuro, igienico e conforme agli standard di qualità più rigorosi.
Nel mondo della produzione farmaceutica e nutraceutica, la precisione e l’efficienza sono requisiti imprescindibili.
Cosa sono le macchine filler stick?
Le macchine filler stick sono sistemi automatizzati progettati per riempire e sigillare stick pack, ovvero bustine sottili e allungate, perfette per la monodose.
Questi formati (confezionamento stick pack) sono sempre più apprezzati per la loro praticità, sia in ambito OTC (over-the-counter) che in quello professionale, come cliniche, laboratori e farmacie.
Nel confezionamento farmaceutico, queste macchine trovano largo impiego nel processo di produzione di:
- Integratori alimentari in polvere (es. vitamine, sali minerali, probiotici);
- Preparati solubili per uso orale;
- Polveri antibiotiche o antipiretiche monodose;
- Soluzioni e sospensioni liquide ad uso orale.
Nel settore nutraceutico e del confezionamento di farmaci, gli stick pack sono il formato ideale per consumatori attenti alla salute e in cerca di praticità d’uso.
Sono ideali per i prodotti da assumere fuori casa o in momenti specifici della giornata, come energy booster, integratori sportivi, o prodotti per il benessere intestinale.
Sanificazione delle macchine filler stick: un aspetto critico per la qualità del prodotto
Nel contesto farmaceutico e nutraceutico, la sanificazione delle macchine filler stick non è un semplice passaggio operativo, ma un punto critico di controllo (CCP) nella garanzia della qualità del prodotto finito.
La natura stessa dei prodotti trattati (spesso altamente igroscopici, termolabili o microbiologicamente sensibili) impone protocolli di igiene rigorosi, validati e sistematicamente verificabili.
Filler stick: tecniche e protocolli di sanificazione
La sanificazione può avvenire secondo diverse modalità, selezionate in base al tipo di prodotto e alla configurazione della macchina:
- CIP (Clean-In-Place): sistema automatizzato che consente il lavaggio interno delle parti a contatto con il prodotto senza smontaggio, mediante l’uso di soluzioni detergenti, disinfettanti e successivo risciacquo con acqua purificata.
- SIP (Sterilize-In-Place): prevede l’uso di vapore saturo per la sterilizzazione dei circuiti, particolarmente importante per applicazioni in asepsi o con ingredienti termicamente resistenti.
- Sanificazione manuale assistita: utilizzata nelle macchine di piccola scala o quando la configurazione non consente il CIP completo; richiede SOP dettagliate e formazione continua degli operatori.
Sanificazione confezionamento prodotti farmaceutici: perché è fondamentale?
Una sanificazione carente o inefficace può portare a:
- Contaminazioni microbiche (batteri, lieviti, muffe), con conseguente rischio per la salute pubblica;
- Cross-contaminazioni tra lotti o prodotti diversi, in particolare in impianti multi-prodotto;
- Compromissione della stabilità del principio attivo o degli eccipienti;
- Non conformità regolatorie, con potenziali blocchi di lotto, richiami dal mercato o sanzioni.
Rischi Associati a una Gestione Igienica Inadeguata
- Perdita di integrità del prodotto e riduzione dell’efficacia terapeutica o nutrizionale;
- Richiami di prodotto e danni reputazionali;
- Impatto sulla shelf-life, con possibili reazioni chimiche o crescita microbica non controllata;
- Non conformità alle normative FDA, EMA, o altre autorità regolatorie, che impongono controlli severi su processi di pulizia e validazione degli impianti.
Rischio di Contaminazione da Biofilm sulle Macchine Filler Stick
Uno dei rischi più insidiosi nella produzione farmaceutica e nutraceutica è la formazione di biofilm sulle superfici a contatto con il prodotto.
Questi aggregati microbici protetti da una matrice extracellulare possono persistere nonostante operazioni di pulizia standard, generando pericoli significativi:
- Resistenza ai disinfettanti: il biofilm esplica una barriera fisica e chimica che rende le popolazioni batteriche fino a 1000 volte più resistenti agli agenti antibatterici rispetto ai batteri planctonici.
- Contaminazione costante: biofilm maturi rilasciano continuamente cellule microbiche (dispersione), contaminando successivi lotti e provocando cross-contaminazione persistente.
- Microrganismi coinvolti: studi nel settore alimentare identificano superfici processate frequentemente contaminate da batteri come Listeria monocytogenes, Staphylococcus aureus, Escherichia coli, Pseudomonas spp. e. Analogamente, in ambito farmaceutico si registrano colonizzazioni da Staph. epidermidis, Propionibacterium e contemporaneamente da altre specie resistenti ai trattamenti.
- Effetti sul prodotto finito: la contaminazione microbica può causare:
- degradazione degli ingredienti attivi e alterazioni della stabilità chimica;
- insorgenza di infezioni o reazioni immunitarie nel consumatore;
- riduzione della shelf-life e non conformità ai requisiti GMP.
La presenza di biofilm su filler stick rappresenta un pericolo silente ma significativo.
Senza adeguati sistemi CIP/SIP, design igienico delle superfici, protocolli di monitoraggio microbiologico e convalidati test di rimozione, le macchine diventano fonti croniche di contaminazione, con ripercussioni su sicurezza del consumatore, qualità del prodotto e conformità normativa.
Gestione del rischio da contaminazioni di biofilm tramite approccio enzimatico con BILISS®: un caso di studio del team Piramide
Le macchine filler stick, specialmente se impiegate nel confezionamento medicinali di liquidi o gel, risultano di difficile detersione e sanificazione per la complessità delle macchine stesse.
Solitamente sono costituite sostanzialmente da:
- Rulli, istallati nella parte posteriore della macchina, su cui sono avvolte le bobine dei materiali che costituiranno le confezioni;
- Tramoggia di carico prodotto;
- Filler
I filler a loro volta sono composti da:
- Formatori (degli stick)
- Dosatori
- Otturatori.
Durante un audit presso un’azienda farmaceutica con delle problematiche di contaminazioni a spot sul prodotto finito in stick da parte di Pseudomonadacee, proprio dallo studio della Filler emergono alcuni punti critici, più precisamente:
- Formatori (parte esterna dei filler) su cui si avvolge il materiale costituente lo stick che successivamente viene saldato alle due estremità per generare lo stick stesso;
- Dosatori;
- Otturatori che caricano il prodotto nella confezione.
In generale, una delle criticità osservate riguardanti i protocolli di cleaning della Filler Stick è la difficoltà di detergere e sanificare tali equipment in CIP, sia per mancanza di vessel di carico a bordo macchina, sia per la mancanza di sistema di captazione degli otturatori o “falsi stick” in grado di tenere i dosatori aperti, ma confinati in apposite capsule per riprendere la soluzione igienizzante.
Date queste criticità, supportati inoltre dai dati raccolti dal cliente tramite analisi microbiologiche nei vari step di produzione, viene individuata proprio la Filler Stick come potenziale punto da cui potrebbe avere origine la contaminazione causata da un potenziale biofilm.
Il trattamento con BILISS® è stato effettuato su due equipment differenti, ma entrambi sospettati per essere contaminati da biofilm. Uno è adibito al riempimento di integratori, l’altro di un farmaco.
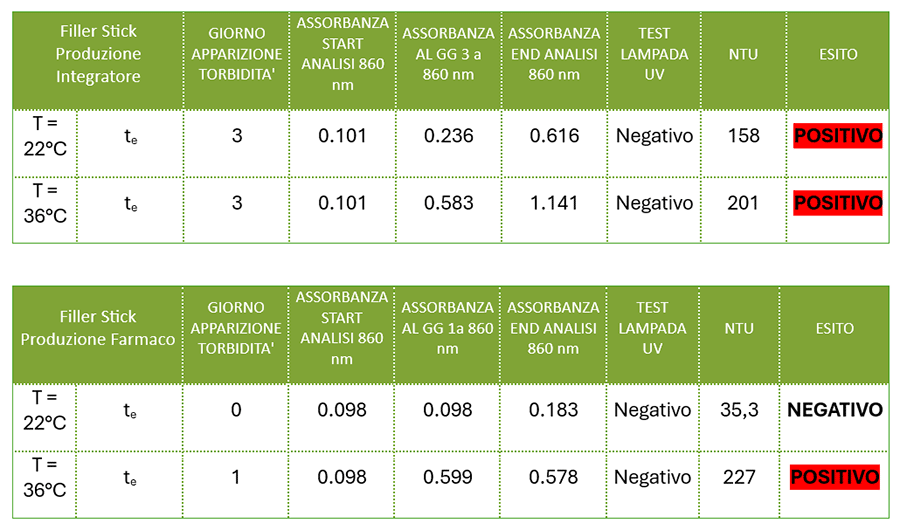
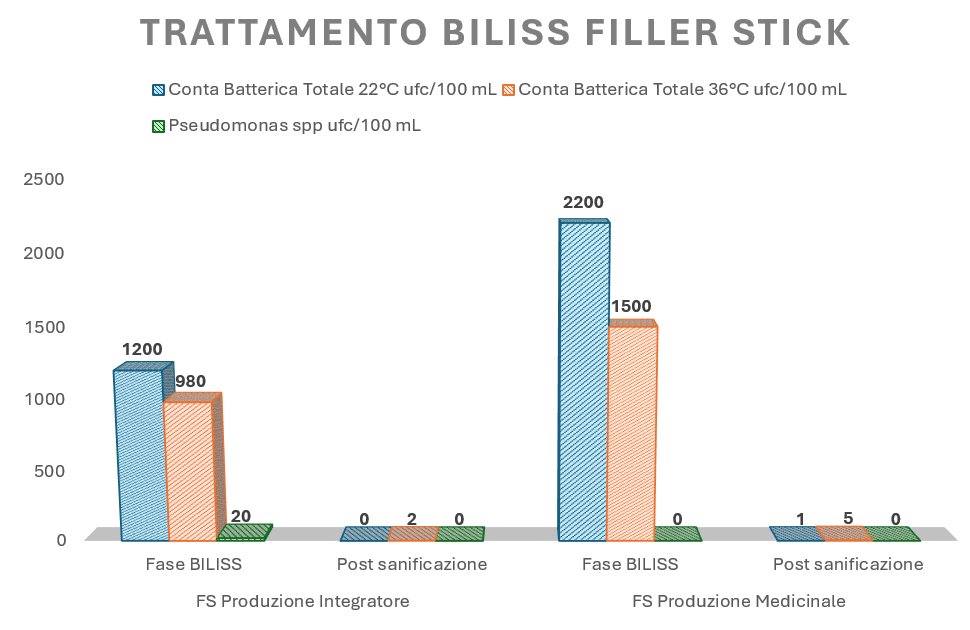
Come da prassi, durante l’assistenza del nostro team di tecnici presso il cliente, sono stati svolte tutta una serie di campionamenti al fine di poter valutare l’effettiva presenza di biofilm sulle macchine trattate, eventuali criticità pretrattamento e infine l’efficacia del trattamento.
Grazie alle analisi svolte è stato possibile dimostrare che entrambe le Filler Stick presentavano una contaminazione da biofilm, confermando anche la presenza di Pseudomonas spp.
Le analisi condotte hanno permesso anche di valutare delle criticità nei protocolli di cleaning giornalieri, e sono stati quindi proposti dei protocolli specifici e ottimizzati, suggerendo sia dei prodotti enzimatici specifici che migliorino l’efficienza di detersione, compensando le criticità descritte prima, sia delle modalità operative che permettano di coinvolgere tutte le parti della macchina.